MSD отозвала из госреестра молнупиравир для лечения COVID-19
Компания MSD отозвала из госреестра противовирусный препарат «Лагеврио» (МНН молнупиравир). Всего Минздрав исключил из госреестра 14 регистрационных удостоверений лекарств и одно РУ на фармсубстанцию. Из исключенных препаратов 10 РУ принадлежат компании АО «Татхимфармпрепараты». Большинство препаратов имеют на российском рынке аналоги.
 Из госреестра отозваны 15 регистрационных удостоверений (РУ). Информация об этом была опубликована на сайте ГРЛС 28 февраля 2023 года. Большинство РУ принадлежат компании АО «Татхимфармпрепараты». Среди компаний владельцев числятся также Krka, Sanofi Innotech International, PolyPeptide Labs и MSD.
Из госреестра отозваны 15 регистрационных удостоверений (РУ). Информация об этом была опубликована на сайте ГРЛС 28 февраля 2023 года. Большинство РУ принадлежат компании АО «Татхимфармпрепараты». Среди компаний владельцев числятся также Krka, Sanofi Innotech International, PolyPeptide Labs и MSD.
Регуляторные решения в отношении всех лекарств вынесены на основании заявлений от владельцев регистрационных удостоверений или их уполномоченных представителей.
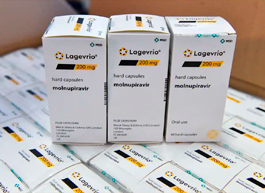
Компания MSD (в США и Канаде — Merck&Co) отозвала из реестра препарат «Лагеврио» (МНН молнупиравир) – применяется при COVID-19. В реестре зарегистрированы семь РУ с действующим веществом молнупиравир. «Лагеврио» был одобрен Минздравом в марте 2022 года. По данным ГРЛС, регистрационное удостоверение действует до 01.01.2024 года. По данным AlphaRM, «Лагеврио» в 2022 году занимал более 22% на российском фармрынке среди лекарств с молнупиравиром. Противовирусное средство закупают для нужд ЛПУ, однако 1% продаж в 2022 году приходился на аптечный рынок.
Из реестра также исключен препарат «Атрикан 250» (МНН тенонитрозол), который применяется в качестве противопротозойного средства при трихомониазе мочеполовой системы. В реестре с таким МНН больше зарегистрированных лекарств нет.
Также из реестра отозвали противоязвенный препарат компании Sanofi «Ультоп» (МНН омепразол). Исключен «Ультоп» в форме лиофилизата для приготовления раствора для инфузий. В реестре есть препараты других производителей омепразола в данной форме. «Ультоп» в России по-прежнему зарегистрирован в виде капсул.
Также в нашей стране теперь невозможно обращение диуретика «Лазикс» (МНН фуросемид) от компании Sanofi в виде раствора для инъекций. О дефиците «Лазикса» сообщали еще в 2020 году. Тогда стало известно, что препарат в инъекционной форме больше не производят.
Российская компания АО «Татхимфармпрепараты» отозвала из реестра 10 РУ на препараты: «Эритромицин», «Рибоксин», «Пирацетам», «Пилокарпин», «Нафтизин», «Левомицетин» глазные капли, «Камфорный спирт», «Диклофенак», «Борная кислота», «Аскорбиновая кислота с глюкозой».
Из реестра исключены следующие лекарственные препараты:
- «Эритромицин» (эритромицин) таблетки, РУ — ЛСР-007901/08 от 07.10.2008;
- «Ультоп» (омепразол), лиофилизат для приготовления раствора для инфузий, РУ — ЛСР-002262/07 от 17.08.2007;
- «Рибоксин» (инозин), таблетки, РУ — ЛП-000240 от 16.02.2011;
- «Пирацетам» (пирацетам), таблетки, РУ — Р N003484/01 от 21.05.2009;
- «Пилокарпин» (пилокарпин), капли глазные, РУ — ЛСР-010622/08 от 26.12.2008;
- «Нафтизин» (нафазолин), капли назальные, РУ — ЛСР-001477/09 от 03.03.2009;
- «Левомицетин» (хлорамфеникол), капли глазные, РУ — ЛС-002068 от 01.11.2011;
- «Лазикс» (фуросемид), раствор для в/в и в/м введения, РУ — П N014865/02 от 16.05.2008;
- «Лагеврио» (молнупиравир), капсулы, РУ — ЛП-007987 от 25.03.2022;
- «Камфорный спирт» (камфора), раствор для наружного применения, РУ — Р N003130/01 от 09.10.2008;
- «Диклофенак» (диклофенак), гель, РУ — ЛП-000306 от 17.02.2011;
- «Борная кислота» (борная кислота), раствор для местного применения, РУ — ЛСР-006589/08 от 14.08.2008;
- «Атрикан 250» (тенонитрозол), капсулы, РУ — П N014806/01 от 29.07.2011;
- «Аскорбиновая кислота с глюкозой» (аскорбиновая кислота+декстроза), таблетки, РУ — ЛСР-004893/09 от 19.06.2009.
Также Минздрав отменил регистрацию фармсубстанции «Атозибан» (атозибан), субстанция-порошок, РУ — ФС-001998 от 15.01.2020.
Атозибан включен в состав лекарств, которые применяют в гинекологии при преждевременных родах. Препарат подавляет сократимость матки. В ГРЛС PolyPeptide Labs числится единственным производителем этой субстанции. В качестве действующего вещества атозибан входит в состав четырех разных препаратов с действующим РУ.
Источник: «Фармацевтический вестник»
- Поделиться:
Главный редактор — Т. Ю. Ходанович. Тел: +7 (495) 120-44-34, email: hello@pharmedu.ru
Публикация № P-36150
