- Популярные теги
-
- #статистика
- #новый препарат
- #COVID-19
- #лекарства
- #коронавирус
- #рейтинги
- #маркировка
- #регуляторика
- #Минздрав
- #МДЛП
- #вакцина
- #ЖНВЛП
- #мигрень
- #терапия
- #аналитика
- #Росздравнадзор
- #Законопроект
- #дженерик
- #Профилактика
- #Аптеки
- #отзыв
- #БАД
- #интернет-торговля
- #аптечные сети
- #ФАС
- #Профилактика заболеваний
- #неврология
- #исследования
- #продажи
- #диабет
- #Согласование цен
- #клинические исследования
- #безопасность лекарств
- #сертификация
- #онкология
- #промомед
- #инфекции
- #аккредитация
- #инструкция
- #ПСК Фарма
- #аллергология
- #вакцина от COVID-19
- #мерчендайзинг
- #Герофарм
- #дефицит лекарств
- #психология
- #педиатрия
- #Грипп
- #антибиотики
- #лекарственная терапия
- #дефектура
- #лечение COVID-19
- #ВОЗ
- #управление аптеками
- #новые формы
- #Роспотребнадзор
- #ВИЧ
- #Вакцинация
- #Правительство
- #мнение специалиста
- #новые показания
- #Клинические рекомендации
- #контрацепция
- #НМО
- #эндокринология
- #ПКУ
- #рынок лекарств
- #Суд
- #льготные рецепты
- #Р-Фарм
- #деменция
- #Петровакс Фарм
- #рецепты
- #разработка
- #Витамин D
- #вирусы
- #заболевания сердца
- #побочный эффект
- #семаглутид
- #российский рынок
- #хирургия
- #Одобрение
- #иммунология
- #акушерство-гинекология
- #Здравоохранение
- #ожирение
- #болезнь Паркинсона
- #Акрихин
- #Сервье
- #поступление в оборот
- #вирус
- #Госдума
- #офтальмология
- #Валента Фарм
- #туберкулез
- #Второй лишний
- #Генериум
- #кардиология
- #Госзакупки
- #Фармасинтез
- #беременность
- #фармакология
- #оригинальное лекарство
- #Минпромторг
- #опрос
- #урология
- #FDA
- #Novo Nordisk
- #диагностика
- #Боль
- #Эндофарм
- #ревматоидный артрит
- #рекомендации по питанию
- #питание
- #Озон Фармацевтика
- #Roche
- #остеопороз
- #профилактика COVID-19
- #Eli Lilly
- #иммунитет
- #нейролептики
- #Pfizer
- #Безен Хелскеа
- #прекращение поставок
- #контроль заболевания
- #НПВП/НПВС
- #стресс
- #кишечные инфекции
- #психиатрия
- #рак легких
- #слияние и поглощение
- #упаковка
- #ХимРар
- #инсульт
- #нейроинфекция
- #Полисан
- #пульмонология
- #гастроэнтерология
- #Ростех
- #атопия
- #Гедеон Рихтер
- #бронхиальная астма
- #нанолек
- #целиакия
- #бактериофаги
- #сердечная недостаточность
- #геронтология
- #грибковые инфекции
- #ССЗ
- #Министерство
- #АСНА
- #Биннофарм
- #анемия
- #дети
- #язвенный колит
- #тромбоз
- #оториноларингология
- #Профилактика ССЗ
- #меланома
- #Молодые специалисты
- #Производитель
- #орфанные заболевания
- #иммунизация
- #лечение ожирения
- #Байер
- #аутизм
- #болезнь Альцгеймера
- #гепатология
- #рынок труда
- #уголовное дело
- #опухоль
- #когнитивные нарушения
- #Эксперимент
- #хроническая болезнь почек
- #критерии
- #Генная терапия
- Показать все теги
Минобороны завершило испытания вакцины от COVID-19 на добровольцах
Первая российская вакцина от коронавируса готова, у всех добровольцев, участвовавших в клинических испытаниях, выработались антитела, сообщил первый замминистра обороны Руслан Цаликов. Испытания проводились на базе госпиталя имени Бурденко. Вакцина была разработана совместно Минобороны и Национальным исследовательским центром эпидемиологии и микробиологии имени Гамалеи.
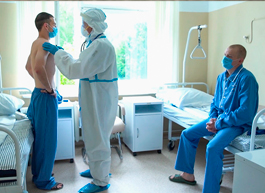 В составе группы были 20 человек. Им вводили вакцину, разработанную совместно Министерством обороны и Национальным исследовательским центром эпидемиологии и микробиологии имени Н.Ф.Гамалеи.
В составе группы были 20 человек. Им вводили вакцину, разработанную совместно Министерством обороны и Национальным исследовательским центром эпидемиологии и микробиологии имени Н.Ф.Гамалеи.
Когда начнется вакцинация населения, не уточняется. «Ученым еще предстоит огромный пласт аналитической работы», — заявил российский военный биолог Сергей Борисевич.
«Ученым еще предстоит огромный пласт аналитической работы, составление итоговых отчетов, представление результатов, государственная регистрация вакцинного препарата. Но уже сейчас имеющиеся данные анализов подтверждают, что в результате вакцинации у добровольцев выявлены необходимые антитела к коронавирусу, а компоненты вакцины безопасны и хорошо переносимы человеком», — подвел итоги клинических испытаний Борисевич.
Он также сообщил, что антитела, дающие организму иммунитет к коронавирусу, сохранятся после введения вакцины надолго. «Возможности платформы, на которой до этого были разработаны две вакцины против лихорадки Эбола и вакцина против Ближневосточного респираторного синдрома, позволят длительно поддерживать защитный титр, вырабатываемый после иммунизации», — сказал Борисевич.
В ходе исследований была использована методология количественной оценки возбудителя, которая была разработана в 48-м ЦНИИ, уточнил начальник института. Также медики использовали лабораторную модель, которая позволила воспроизвести протекание заболевания для оценки защитной эффективности лекарств.
Клинические испытания на добровольцах в госпитале имени Бурденко начались 18 июня. Первая группа, которой ввели вакцину, состояла из 18 человек. Второй группе ввели препарат через несколько дней после того, как результаты первых клинических испытаний позволили продолжить исследования.
В конце июня добровольцы сообщали, что чувствуют себя хорошо, никаких побочных явлений или осложнений выявлено не было.
Источник: РБК
- Поделиться:
Главный редактор — Т. Ю. Ходанович. Тел: +7 (495) 120-44-34, email: hello@pharmedu.ru
Публикация № P-34722